La spectrophotométrie d’absorption atomique
Principe
La spectrophotométrie d’absorption atomique (SAA , Atomic Absorption Spectroscopy AAS) est une méthode de dosage exclusivement d’éléments métalliques, il n’y a pas de spectres à proprement parlé : Aspect quantitatif seulement.
Un rayonnement électromagnétique monochromatique est envoyé sur la population d’atomes à doser mis à l’état de vapeur. Ces atomes vont absorber une partie du rayonnement. La mesure de I0 et It permet de connaître la concentration de l’élément à doser:
(1) ![]()
Appareillage
Tout instrument d’absorption atomique contient les mêmes éléments de base, à savoir :
- Une source de lumière (source primaire) qui produit une radiation caractéristique de l’élément à doser à la longueur d’onde
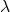
- un système pour moduler le rayonnement provenant de la source
- d’un diviseur de faisceau lumineux dans les appareils à double faisceau
- un atomiseur dont le rôle est de produire un nuage d’atomes à l’état fondamental
- un monochromateur sert à éliminer toutes les radiations autres que celle à la longueur d’onde
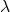 choisie
choisie - un détecteur couplé à un système électronique pour enregistrer et traiter les signaux.
Schéma de principe
Il existe, suivant les constructeurs et les gammes d’appareils, des spectromètres à simple ou double faisceau.
Dans les spectromètres à simple faisceau, la lumière issue de la source traverse l’atomiseur et le monochromateur pour aboutir directement sur le détecteur.
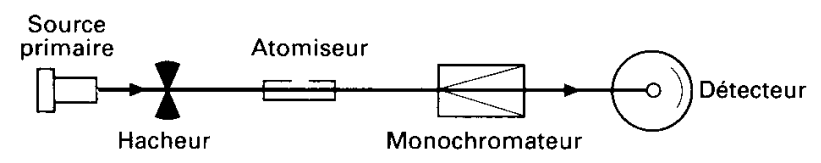
Soit ![]() l’intensité lumineuse du rayonnement à la longueur d’onde caractéristique de l’analyte. Le long du trajet optique, cette intensité est atténuée non seulement par l’analyte, mais aussi éventuellement par l’air en dehors de l’atomiseur, par l’atomiseur lui-même (la flamme surtout) et par les composants optiques. Un réglage du zéro, en faisant une mesure en l’absence d’échantillon, permet de corriger ces atténuations indésirées à condition d’être certain de la stabilité de l’alimentation électrique de l’installation ainsi que de la stabilité de l’atomiseur.
l’intensité lumineuse du rayonnement à la longueur d’onde caractéristique de l’analyte. Le long du trajet optique, cette intensité est atténuée non seulement par l’analyte, mais aussi éventuellement par l’air en dehors de l’atomiseur, par l’atomiseur lui-même (la flamme surtout) et par les composants optiques. Un réglage du zéro, en faisant une mesure en l’absence d’échantillon, permet de corriger ces atténuations indésirées à condition d’être certain de la stabilité de l’alimentation électrique de l’installation ainsi que de la stabilité de l’atomiseur.
Dans les spectromètres à double faisceau, le faisceau incident est divisé en deux parties, un faisceau traversant l’atomiseur, l’autre, de référence, contournant l’atomiseur. Ce faisceau subit les atténuations dues à l’air et aux pertes de lumière, mais pas celles dues à l’absorption par l’atomiseur. Le faisceau de référence permet surtout de tenir compte des fluctuations de l’émission de la source.
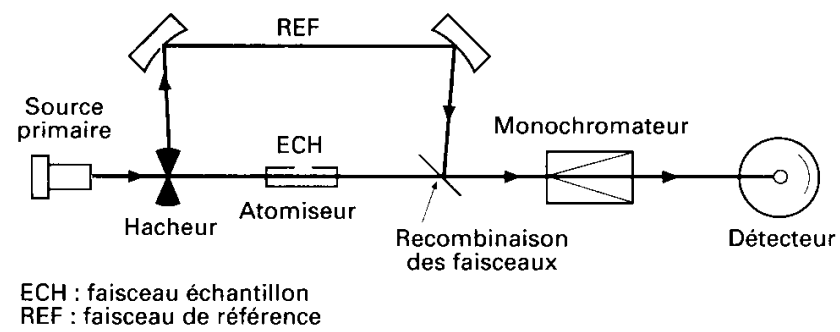
Les deux faisceaux sont recombinés à l’entrée du monochromateur. Le détecteur reçoit alternativement ces deux faisceaux. L’intensité du faisceau de référence est prise comme ![]() .
.
Sources de radiations
Lampe à cathode creuse
Les lampes à cathode creuse (Hollow Cathode Lamps, HCL) sont certainement les lampes les plus répandues,
Le principe de fonctionnement est toujours le même.
Les lampes sont constituées :
- d’un tube en verre d’une vingtaine de centimètres de long et de 3 à 5 cm de diamètre, fermé à l’extrémité par une fenêtre de quartz transparente aux UV ;
- d’une anode en tungstène (W) généralement;
- d’une cathode cylindrique en forme de petit godet d’environ 1 cm de profondeur et de 3 à 5 mm de diamètre. Le fond de la cathode, qui est la partie essentielle de la lampe, est usinée en l’élément que l’on veut doser, ou recouvert de l’élément ou d’un alliage de celui-ci.
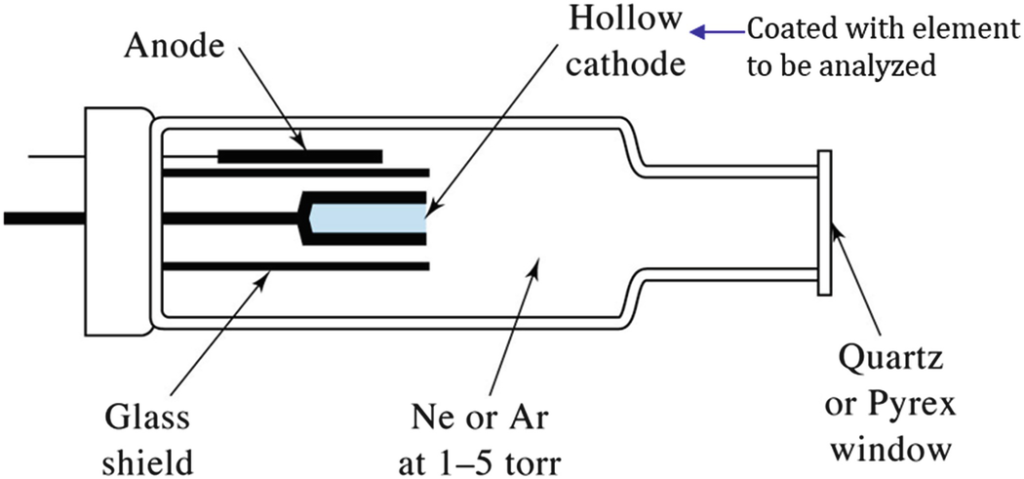

L’air a été évacué hors de la lampe et remplacé par un gaz inerte, Ne ou Ar, sous faible pression. (0,5 à 1,3 kPa).
Une différence de potentiel comprise entre 100 et 400 V est appliquée entre l’anode et la cathode. Une décharge va apparaître entre les deux électrodes et cette décharge sera concentrée dans la cathode qui va émettre des électrons hautement énergétiques. Ces électrons vont entrer en collision avec les atomes du gaz de remplissage et vont l’ioniser, par exemple :
(2) ![]()
Les ions ![]() ou
ou ![]() vont ensuite être attirés par la cathode en subissant une accélération importante. L’accélération va leur conférer une énergie cinétique telle que, en percutant le fond de la cathode, ils arracheront un atome de celle-ci.
vont ensuite être attirés par la cathode en subissant une accélération importante. L’accélération va leur conférer une énergie cinétique telle que, en percutant le fond de la cathode, ils arracheront un atome de celle-ci.
Les vapeurs métalliques confinées dans la cathode sont soumises à un flux intense d’ions argon (ou néon) mais aussi d’électrons. Il en résulte un grand nombre de collisions avec, pour conséquence, le passage à l’état excité des atomes métalliques. De l’état excité, ils vont redescendre à l’état fondamental en émettant chacun un photon dont l’énergie dépendra de l’état excité auquel l’atome aura été porté.
(3) ![]()
La lumière émise par la lampe n’est donc pas monochromatique, mais est constituée de plusieurs raies caractéristiques de l’élément. Parmi celles-ci, la plus intense sera celle qui correspond à la transition la plus probable, c’est-à-dire celle qui fait intervenir le premier niveau excité, à la longueur d’onde ![]() . À ces raies s’ajoutent aussi celles du gaz de remplissage.
. À ces raies s’ajoutent aussi celles du gaz de remplissage.
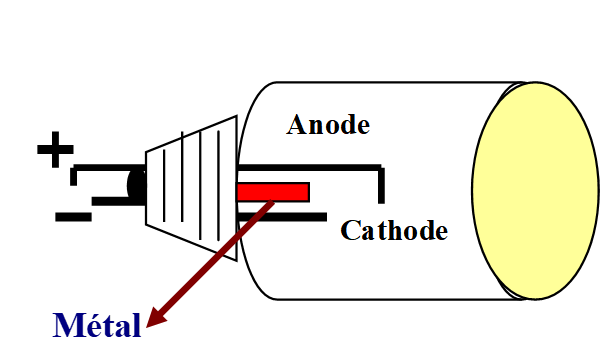
Lampes à vapeur métallique
Elles utilisent l’émission lumineuse produite par une décharge électrique dans des gaz sous pression réduite.
Cette lampe contient l’élément métallique à l’intérieur. il y a une anode et une cathode ; l’élément métallique doit être volatilisable à la chaleur ( Ex : Hg, Na).
Les lampes à décharge de vapeur de mercure par exemple sont utilisées dans les appareils d’absorption atomique qui sont dédiés au dosage de ce métal.
Lampes à décharge sans électrode
Le principe de fonctionnement des lampes EDL est très proche de celui d’un plasma induit (ICP), sauf que les températures sont beaucoup plus faibles.
Les lampes HCL et EDL sont parfaitement complémentaires, les premières donnant d’excellents résultats pour les métaux non volatils, les secondes s’adressant particulièrement bien à l’étude des métaux volatils (As, Bi, Ge, Pb, Sb, Se, Sn).
Modulateur
Il permet d’interrompre le faisceau incident de manière transitoire :
- Interruption mécanique : par un demi-disque tournant appelé aussi hacheur
- Interruption électrique : la cathode est alimentée par un courant alternatif, 2 intérêts :
- Il est plus aisé de mesurer un signal alternatif qu’un signal continu
- Intérêt principal : distinguer les photons émis par l’élément des photons émis par la source et non absorbés.
Explication : le rayonnement transmis à partir de la cathode creuse (courant alternatif) est différent du rayonnement émis par les atomes qui reviennent à l’état fondamental (courant continu).
Les systèmes d’atomisation
La lumière émise par la source primaire passe au travers de la cellule d’absorption (l’atomiseur) où une partie de la lumière incidente est absorbée. Étant donné que le rayonnement incident provient de transitions atomiques d’un élément, il ne peut être absorbé que par des atomes de cet élément (ou une autre espèce qui absorbe à la même longueur d’onde). Or, dans pratiquement tous les cas, et surtout si l’échantillon est en solution, l’élément à doser n’est pas à l’état atomique, mais bien à l’état ionique ou combiné.
Le rôle de l’atomiseur est de produire des atomes, mais ceux-ci doivent se trouver à l’état fondamental pour pouvoir absorber les photons provenant de la source. On distingue essentiellement deux types d’atomiseurs : la flamme (SAA en flamme) et le four en graphite (SAA électrothermique).
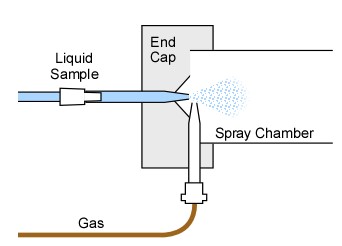
Nébuliseur
Avant d’arriver dans le brûleur, la solution doit être transformée en un fin brouillard lors d’une étape primordiale : la nébulisation.
Celle-ci a cependant un rendement médiocre : la majeure partie de la solution est évacuée sous forme de grosses gouttelettes par le drain ; seuls environ 10 \% atteignent réellement la flamme. Idéalement, il
faudrait que les gouttelettes dans l’aérosol aient un diamètre inférieur à 1 [/latex]\mu[/latex]m .
Il existe 2 principaux type de nébuliseurs, le nébuliseur pneumatique et le nébuliseur ultrasonique.
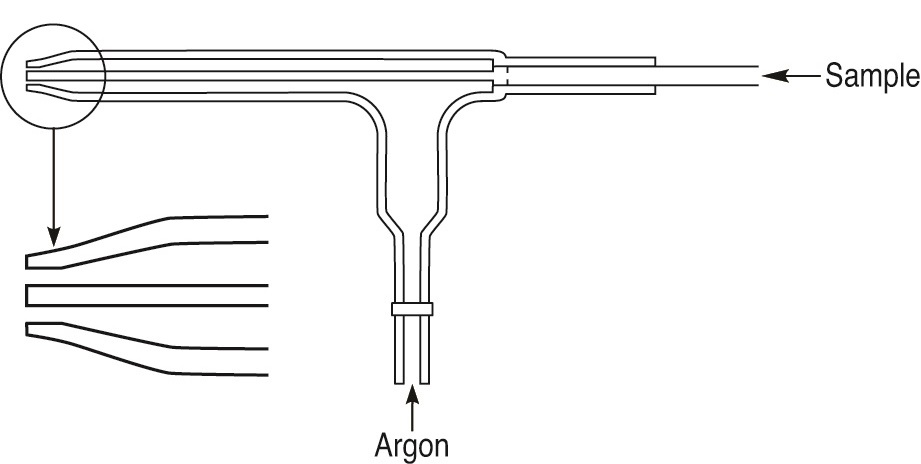
- Nébuliseur Pneumatique : Le plus souvent utilisé en SAA, le liquide sort du capillaire à vitesse élevée suite à un jet gazeux à grande vitesse de façon tangentielle ou axiale à la surface du liquide, ce qui provoque déjà un début de nébulisation. Le brouillard formé va encore être divisé en plus fines gouttes. soit par le combustible qui arrive à contre-courant, soit par une bille d’impact ou encore une hélice de triage qui divise les gouttes. Au-delà de ce lieu de nébulisation se trouve une série de chicanes qui ont pour objet de recondenser les grosses gouttes afin qu’elles soient évacuées par le drain. L’obtention des gouttelettes très fines dépend du débit du gaz, du débit du liquide, de la viscosité du liquide. L’optimisation de la nébulisation passe par la maitrise de ces paramètres.
- Nébuliseur par ultrasons: Dans le nébuliseur ultrasonique (rarement utilisé en SAA), la solution coule sur un cristal de quartz vibrant.
Flamme
Dispositifs
La flamme est produite à l’aide d’un brûleur alimenté par un mélange combustible/comburant.
Ex: acétylène/air
On distingue deux types:
Brûleur à flamme turbulente = brûleur de diffusion.
- Le carburant et le comburant sont amenés séparément: c’est indispensable quand on a des mélanges gazeux susceptibles d’exploser (oxygène/hydrogène).
- Inconvénient: flammes peu stables.
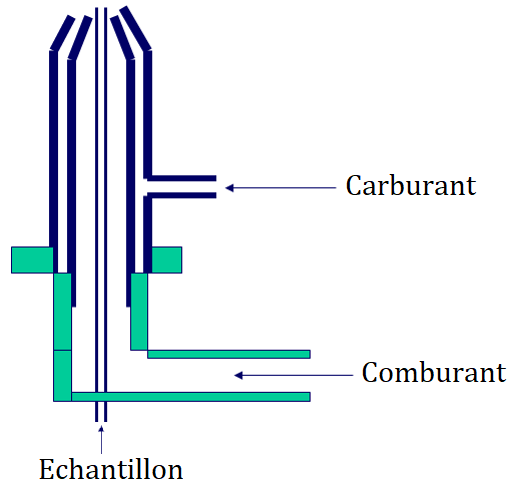

Brûleur à flamme laminaire = brûleur de pré-mélange:
seul utilisé dans les appareils récents.
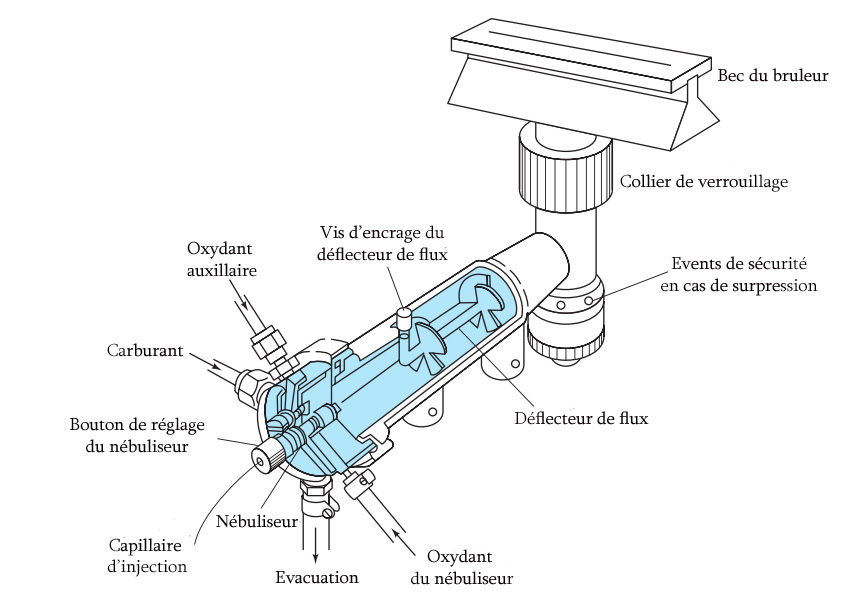
- Les gaz sont mélangés avant l’arrivée dans la flamme ; il y a une enceinte de pré-mélange.
- La flamme est beaucoup plus stable du fait du pré-mélange.
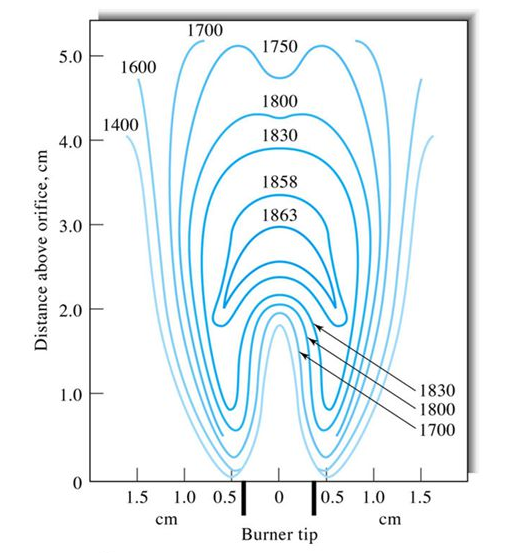
Au cours de l’analyse, on aura la succession de plusieurs phénomènes.
Phénomènes physico-chimiques
Au cours de l’analyse on aura la succession de plusieurs phénomènes: voir figure
![]()
Mélange de gaz
Il faut un carburant et un comburant. On choisit le mélange de gaz en fonction de la température nécessaire pour obtenir l’atome à l’état de vapeur.
Exemple :
- Na (1800 °C)
 butane ou propane
butane ou propane - Al (plus de 2000 °C)
 hydrogène
hydrogène
| Mélange combustible/comburant | T°C max |
| butane/air | 1700 – 1900 °C |
| propane/air | 1915°C |
| hydrogène/air | 2100 °C |
| hydrogène/oxygène | 2850 °C |
| acétylène/air | 2125 – 2400 °C |
| acétylène/protoxyde d’azote (N2O) | 2950°C |
Les gaz qui entretiennent la flamme sont un mélange de comburant et de combustible. Le comburant est le plus souvent l’air et, dans certains cas, le protoxyde d’azote N2O.
Les combustibles sont surtout l’acétylène, parfois le propane ou l’hydrogène. C’est l’acétylène qui fournit les flammes les plus chaudes. La flamme la plus couramment utilisée est donc la flamme air-acétylène (2500 °C). Suivant le rapport air/acétylène, on aura une flamme pauvre (en acétylène), stœchiométrique ou riche.
La flamme pauvre est oxydante et sa température est élevée. La flamme riche est réductrice et sa température est moindre. Le caractère oxydant est dû à la présence d’un excès d’oxygène et le caractère réducteur au fait que, la combustion n’étant pas directement totale, il y a dans la flamme des entités réductrices telles que des atomes de carbone. La présence d’oxygène ou d’espèces réductrices joue un rôle très important dans l’efficacité d’atomisation.
Lorsque la température de la flamme air-acétylène est insuffisante (éléments réfractaires), il convient de remplacer l’air par du protoxyde d’azote.
Le choix des gaz et de leurs proportions dépend de la température à atteindre et du caractère oxydant ou réducteur désiré. Ce choix est conditionné par la nature du métal à doser.
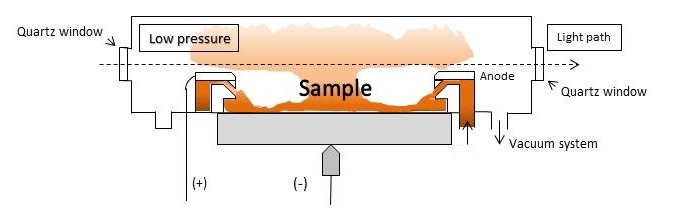
Le four
C’est un tube cylindrique, traversé par le faisceau incident provenant de la lampe utilisée. À l’intérieur, on trouve une petite plate-forme interchangeable (tube en graphite).
Un petit orifice va permettre de réaliser une injection d’un certain volume d’échantillon (1 à 100 [/latex]\mu[/latex]L) sur la plate-forme.
Ce cylindre est chauffé (il se comporte comme une résistance électrique). En même temps, le cylindre est balayé par un gaz inerte (Argon … ) pour le refroidir.
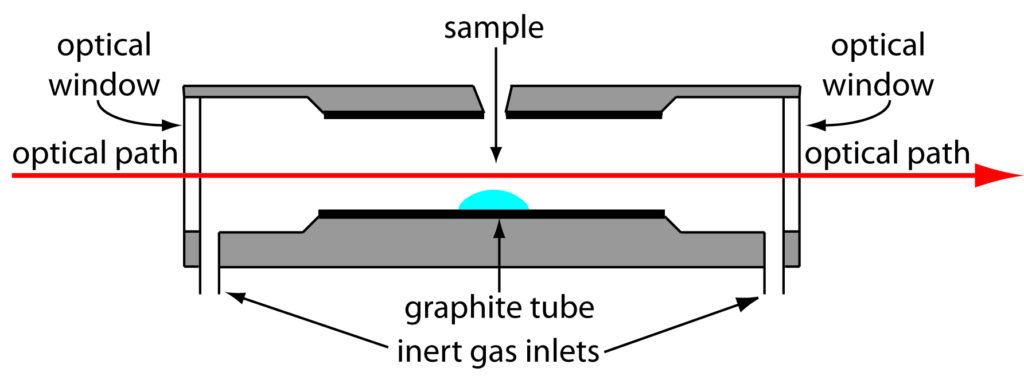

On obtient des atomes à l’état de vapeur.
Les avantages de cette technique sont qu’on travaille en atmosphère inerte sans oxygène (pas de problèmes d’oxydes réfractaires) et la température est programmée en fonction du temps.
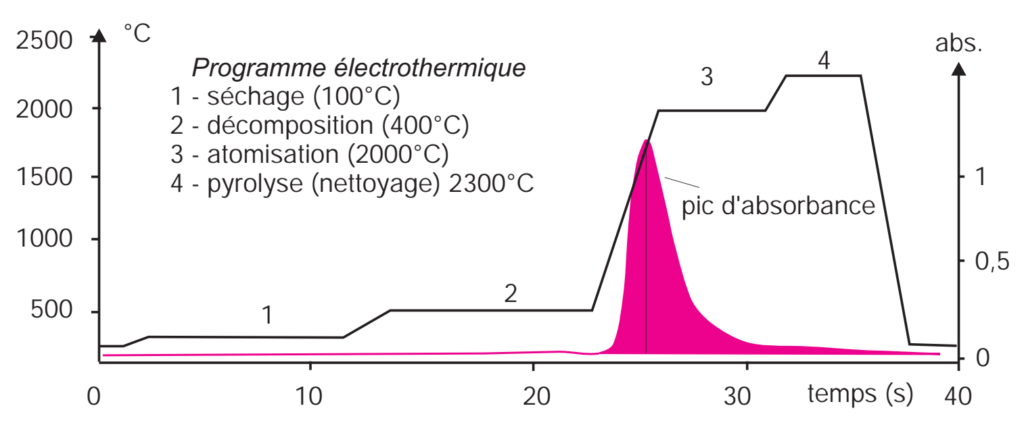
Après l’introduction de l’échantillon à l’intérieur du tube, celui-ci est chauffé suivant un programme thermique (figure ?? ) qui se déroule en trois étapes principales : séchage, décomposition et atomisation.
- Séchage: Pour les solutions aqueuses, le séchage se situe aux environs de 100 °C pendant une durée approximative de 2 s par microlitre de solution.
- Décomposition: L’étape de décomposition (minéralisation, pyrolyse) permet de simplifier la matrice de l’échantillon, d’éliminer les fumées, les vapeurs moléculaires et autres constituants formés lors de la minéralisation des substances organiques. Durant cette étape, des réactions chimiques, telles que la formation d’oxydes ou de carbures, ont également lieu. Elle représente par conséquent l’un des paramètres les plus critiques du programme thermique. La température optimale de décomposition conduit au meilleur rendement d’atomisation.
- Atomisation: L’étape d’atomisation permet de dissocier la matrice résiduelle et d’atomiser le plus sélectivement possible l’élément dosé. La température appliquée et la durée de l’étape doivent être suffisantes pour entraîner l’atomisation complète de l’analyte.
Après l’atomisation, une étape de nettoyage à température élevée permet d’évacuer les résidus subsistant dans le tube.
L’analyse avec un four présente une meilleure sensibilité que la flamme : les vapeurs restent disponibles au REM (dans le cas d’une flamme, il y a dispersion en permanence et perte dans l’atmosphère).
Rappelons que l’absorbance est directement proportionnelle au nombre d’atomes à l’état fondamental dans le faisceau optique au moment de la mesure. Ce nombre d’atomes dépend, bien entendu, de la concentration initiale de l’analyte dans la solution, mais aussi de toute une série d’autres facteurs.
L’atomiseur à tube de graphite est positionné à la place du brûleur et le faisceau lumineux le parcourt dans le sens de la longueur. Les dimensions du four sont d’environ 3 cm de long et 0,5 cm de diamètre. Il est ouvert aux extrémités et est percé d’un orifice au centre de la face latérale pour permettre l’introduction de l’échantillon.
Il faut faire une distinction entre l’introduction de l’échantillon dans une flamme et dans un four : en SAAF, on aspire la solution à débit constant aussi longtemps que nécessaire, tandis qu’en SAAE on dépose 5 à 100 [/latex]\mu[/latex]L de solution dans le four. Dans ce dernier cas, la mesure sera discontinue, ce qui implique un système particulier d’enregistrement du signal, de préférence informatique.
Le tube est tout d’abord en contact électrique avec des électrodes, il est, en effet, chauffé par effet Joule, par passage de courant élevé dans les électrodes suivant un programme de température. Comme la température va être, à un moment donné, portée à plus de 2 000 °C, il faut éviter que le graphite soit en contact avec l’oxygène atmosphérique, sinon il brûlerait instantanément. Pour ce faire, on fait passer, autour et à l’intérieur du tube, un gaz inerte, habituellement l’argon.
Afin d’éviter que le bloc métallique contenant l’alimentation électrique et les conduites de gaz ne s’échauffe : cela est assuré par une circulation d’eau qui refroidit également le four à la fin du cycle.
Dans les premiers atomiseurs électrothermiques, la solution analysée était introduite dans le tube de façon manuelle à l’aide de micropipettes munies d’embouts à usage unique. Le volume d’échantillon varie généralement de 5 à 50 [/latex]\mu[/latex]L. L’utilisation d’un système automatique d’injection améliore dans une large mesure la reproductibilité des dosages. Les injecteurs automatiques récents forment un ensemble avec un distributeur pouvant contenir plusieurs dizaines d’échantillons, des étalons et d’autres solutions à ajouter aux échantillons et aux étalons.
Ainsi, les analyses de routine peuvent se dérouler de façon entièrement automatique sans l’intervention de l’opérateur. Le tube est usiné en graphite (qualité spectrographique, appelé électrographite), dont le point élevé de sublimation permet de supporter des températures voisines de 3 000 °C.
Il peut par contre former des carbures stables ou des composés interstitiels avec certains éléments, rendant ainsi leur atomisation difficile. Un autre défaut du graphite est sa porosité, qui permet l’infiltration de la solution analysée dans les pores et la diffusion à haute température des vapeurs au travers des parois de l’atomiseur. Pour prévenir ces effets indésirables, la surface du tube est recouverte par une pellicule de carbone pyrolytique qui assure l’imperméabilité de la paroi du tube aux solutions et aux gaz.
Au fur et à mesure que le tube vieillit, sa surface pyrolytique se détériore en laissant apparaître le substrat de graphite ordinaire ; la porosité augmente alors progressivement et la formation de carbures devient alors plus probable.
Ce tube présente des effets de mémoire de plus en plus prononcés qui se traduisent par des atomisations peu répétables.
Certains métaux nécessitent des conditions d’atomisation spéciales. On trouve ainsi 2 variantes:
Atomisation des hydrures
Certains éléments : As, Pb, Se, Sb, Bi
Certains éléments sont très difficiles à doser en utilisant un four en graphite. En effet, quelle que soit la matrice, il est pratiquement impossible de décomposer l’échantillon sans perdre l’analyte, tant sa volatilité est grande.
Ces éléments sont surtout As, Ge, Se, Te, auxquels il faut encore ajouter le mercure, bien que son cas se traite différemment. Les cinq éléments que nous venons de citer, ainsi que Bi, Pb, Sb et Sn, ont la propriété de former des hydrures volatils. Tous ces composés sont des gaz à température ambiante.
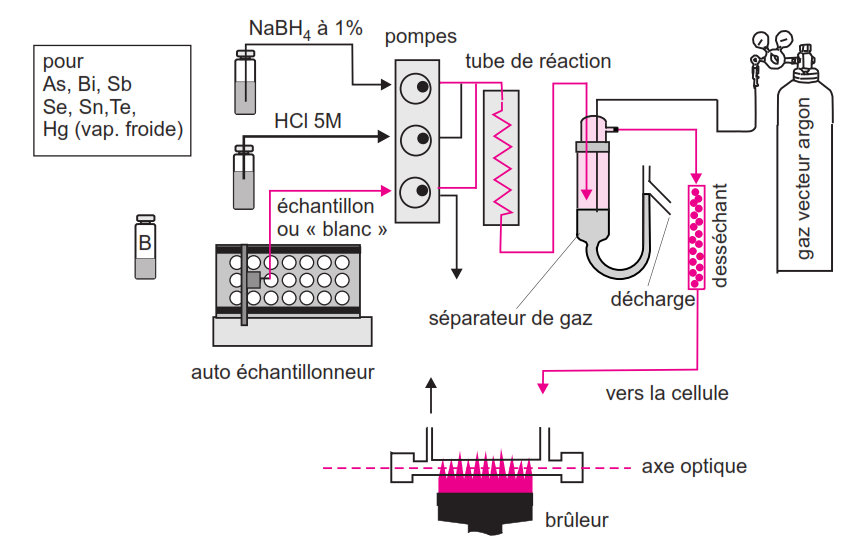
L’installation se compose de deux parties :
- Le générateur d’hydrures proprement dit qui est situé en dehors du spectrophotomètre.
- La cellule d’atomisation qui est placée dans le faisceau optique, à la place de la flamme ou du four.
Une prise d’échantillon (de 1 à 30 mL), acidifiée par HCl est placée dans un flacon de réaction. Dans un premier temps, l’installation est purgée par un courant de gaz inerte de façon à éliminer l’oxygène qui détruirait les hydrures. Du NaBH4 (dans KOH à 2 %) est ensuite introduit dans la solution à analyser. Il se retrouve en milieu acide et se décompose rapidement suivant la réaction :
Au moment de la décomposition, il y a formation d’hydrogène radicalaire, beaucoup plus réactif que l’hydrogène moléculaire.
C’est cet hydrogène radicalaire qui contribue à la formation des hydrures.
L’hydrure formé est entraîné par le courant de gaz vers la cellule d’atomisation. Celle-ci est constituée d’un long tube de quartz d’une quinzaine de centimètres de long, placé, le plus souvent, dans un four chauffé électriquement à température constante de 900 à 1 000 °C. Cette température est suffisante pour décomposer les hydrures et libérer les atomes. Le tube est éclairé par la source primaire de l’élément à doser et le signal d’absorbance est mesuré de façon classique.
Il existe actuellement des systèmes entièrement automatiques de génération d’hydrures.
(4) ![]()
(5) ![]()
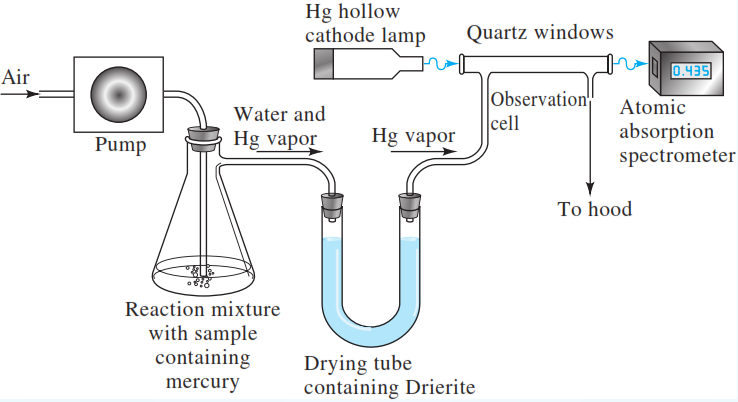
Atomisation de vapeur froide
Le mercure représente un cas tout à fait particulier en SAA. En effet, lors de l’étape de réduction, il se forme directement du mercure métallique à l’état atomique. La pression de vapeur du mercure est suffisante, même à température ambiante, pour qu’il puisse se dégager. C’est la raison pour laquelle on appelle cette technique l’absorption atomique à vapeurs froides.
L’agent réducteur peut être NaBH4 ou encore SnCl2, celui-ci agissant suivant la réaction :
Échantillon : ![]()
(6) ![]()
Cette méthode a amené les constructeurs à concevoir des appareils totalement dédiés à ce dosage.
Système de mesure
Monochromateur
Le rôle du monochromateur consiste à éliminer toute la lumière, quelle que soit son origine, ayant une longueur d’onde différente de celle à laquelle on travaille (généralement la raie de résonance de l’élément à étudier).
Le monochromateur est constitué de trois éléments essentiels :
- Une fente d’entrée chargée de définir un pinceau de lumière polychromatique
- Un système dispersif de la lumière (prisme ou surtout un réseau de diffraction)
- Une fente de sortie chargée de sélectionner la longueur d’onde et de définir la bande passante.
La lumière qui quitte la source (lampe) n’est pas monochromatique : c’est un spectre de raies contenant les raies de l’élément à doser, les raies du gaz de remplissage, ainsi que les raies d’éventuelles impuretés. Les raies de l’analyte vont être en partie absorbées dans l’atomiseur, dans des proportions variables, mais, parmi celles-ci, une seule est intéressante, celle de la transition la plus probable.
D’autre part, l’atomiseur lui-même émet de la lumière. Il y a tout d’abord l’émission propre de l’atomiseur, la flamme par exemple, en l’absence de tout échantillon. Puisque l’atomiseur est suffisamment chaud pour exciter les atomes de l’échantillon, ceux-ci reviennent à l’état fondamental en émettant de la lumière aux longueurs d’onde caractéristiques des éléments constitutifs de l’échantillon. Ces émissions sont d’autant plus intenses que les concentrations de ces éléments sont élevées et que le potentiel d’excitation de ces éléments est faible. Tous les éléments autres que l’analyte émettent à des longueurs d’onde différentes de celle de travail.
La majorité des spectromètres d’absorption atomique ne permet d’analyser qu’un seul élément à la fois. C’est la rotation du réseau, monté sur un plateau tournant, qui assure la sélection de la longueur d’onde par défilement du spectre devant la fente de sortie.
Détecteur
Le détecteur est situé à la sortie du monochromateur. Son rôle est de mesurer les intensités lumineuses nécessaires au calcul des absorbances. Pratiquement tous les appareils à l’heure actuelle sont équipés d’un tube photomultiplicateur. Ce système de détection convient parfaitement pour tous les spectromètres permettant l’analyse monoélémentaire.
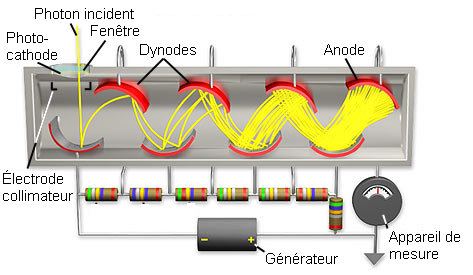
Le photomultiplicateur peut être remplacé par un système de détection dérivé des barrettes de diodes (photodiode).
Share this content:
Table des matières