Spectrophotométrie d’absorption moléculaire Uv – Visible
Les spectres
Caractéristiques générales
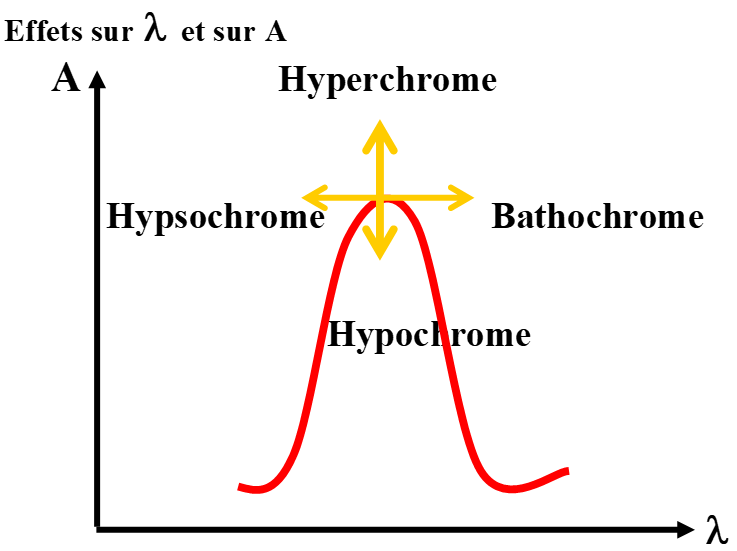
Spectres de bandes : A = f(![]() )
)
niveaux d’énergie électronique
Zone spectrale :
UV: 100 à 400 nm
en pratique, on travaille à partir de 200 nm, car les UV sont absorbés par l’O2 de l’air et par le matériel ( cuve de mesure)
Visible: 400 à 800 nm
Position et intensité des bandes
- L’absorbance est due à certains groupements dits chromophores (portent la couleur).
- L’absorbance peut être modifiée par d’autres groupements chimiques dits auxochromes
Études des différents chromophores.
Définitions:
Un chromophore est une fonction ou un groupe d’atomes qui modifient la fréquence de l’onde U.V. ainsi que l’intensité d’absorption (e). Les quatre termes utilisés sont:
- Effet bathochrome: le chromophore diminue la fréquence d’absorption
- (augmente le
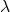 max).
max). - Effet hypsochrome : le chromophore augmente la fréquence d’absorption (diminue le
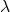 max).
max). - Effet hypochrome : le chromophore diminue l’intensité d’absorption : (diminue
 ).
). - Effet hyperchrome : le chromophore augmente l’intensité d’absorption : (augmente
 ).
).
Groupements chromophores
Ce sont des groupements insaturés qui sont responsable de l’absorption de la molécule.
Exemple:
- groupements éthyléniques C=C; C
 C
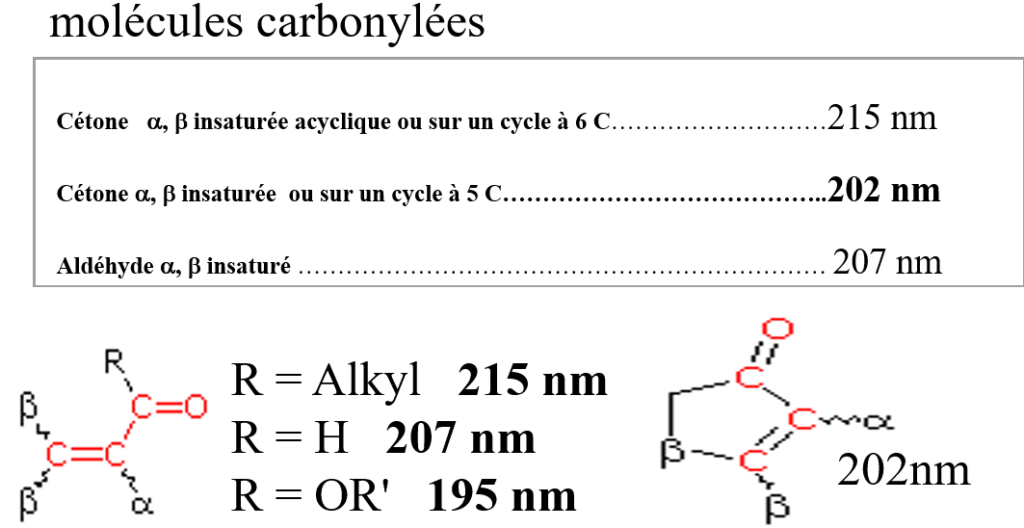
C - groupement carbonyle C = O
Il y a des transitions électroniques:
 *: C = C ; C
*: C = C ; C  C
C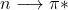 : C = O
: C = O
| Chromophores élémentaires | ||
| Alcène | 173 | 10000 |
| Alcyne | 178 | 2000 |
| Cétone | 290 | 16 |
| Aldéhyde | 279 | 15 |
| Acide | 208 | 32 |
| Chlorure d’acide | 220 | 100 |
| Amide | 220 | 63 |
| Ester | 211 | 57 |
| Nitro | 214 | 17 |
- Transition
 * C=C isolé:
* C=C isolé: 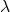 = 170 nm intégré dans une molécule:
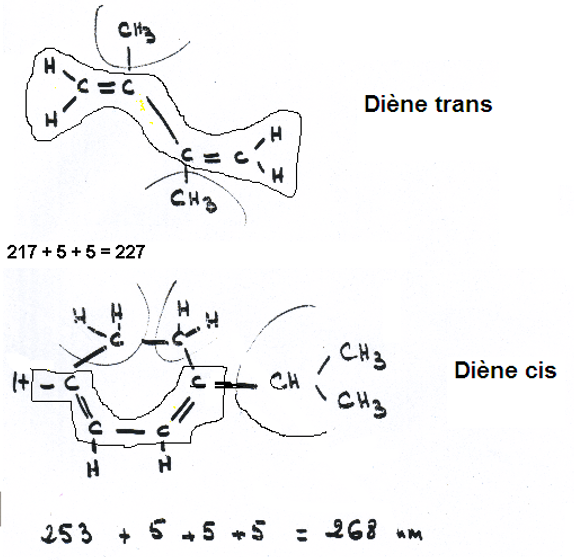
= 170 nm intégré dans une molécule:- Dérivé butadiène trans : 214 nm
- Dérivé butadiène cis : 253 nm
Si les doubles liaisons conjuguées sont plus nombreuses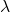 augmente. Exemple: carotène (9 doubles liaisons)
augmente. Exemple: carotène (9 doubles liaisons)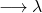 = 590 nm (visible)
= 590 nm (visible)
image inserer = transition1
- Transition
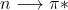 :CH3 – C =O -CH3 Absorbe à 290 nm
:CH3 – C =O -CH3 Absorbe à 290 nm
Autres groupements chromophores:- -C = S 380 nm
- -C = N- 190 nm
Groupements auxochromes
Un auxochrome est, dans une molécule, un groupement d’atomes ionisables pouvant changer la fréquence d’absorption d’un chromophore.
La plupart des auxochromes sont des groupements pouvant former des sels. Ce sont des acides ou des bases susceptibles de se fixer seuls sur le support (colorant réactif) et de résister à la lumière, à l’eau ou au savon.
Auxochromes acides :
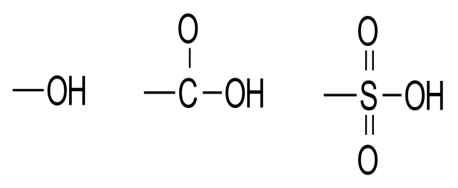
Auxochromes basiques :
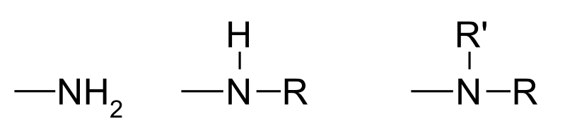
Les éléments halogènes jouent aussi un rôle auxochrome en intensifiant la couleur.
Atomes halogènes :
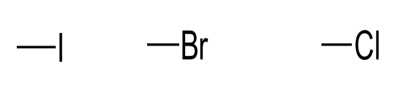
Classement descriptif des bandes d’absorption
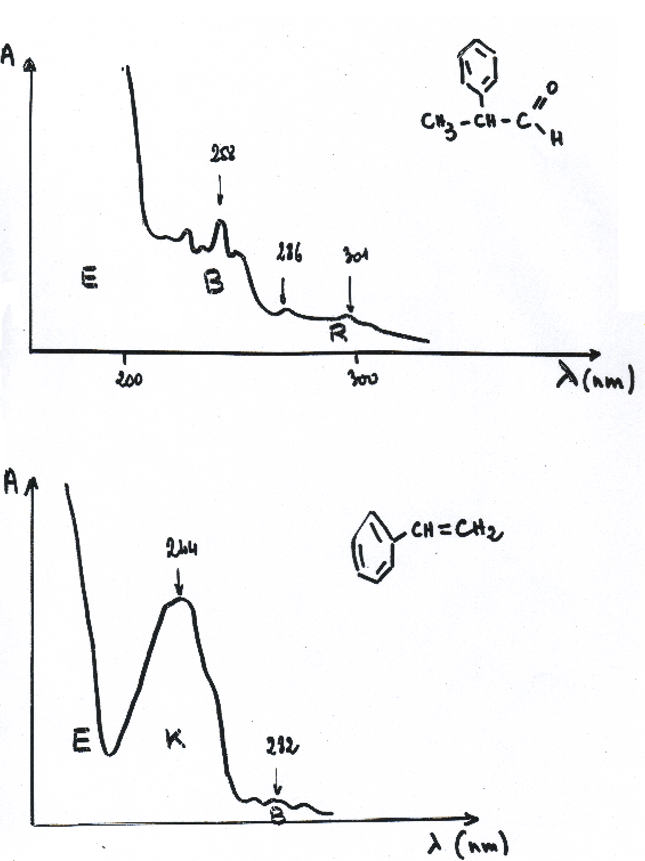
Lors de l’étude d’un spectre UV- visible, on considère 4 types de bandes : E, K, B et R.
- Bandes E comme éthyléniques: dues à des groupements éthyléniques. Elles sont intenses :
 > 10 000
> 10 000
[/latex]\lambda[/latex] située vers les basses longueurs d’onde.
Exemple: 170 nm pour C=C
Elles sont dues aux chromophores C = C ou C C ; transition :
C ; transition :  *
* - Bandes K: bandes de conjugaison (Konjugierte : en allemand):Elles correspondent à des doubles liaisons conjuguées
Transition électronique : *
* élevé: > 10 000
élevé: > 10 000
Elles apparaissent à des longueurs d’onde supérieures à 200 nm
Exemple : butadiène 217 nm C = C — C = C - Bandes B comme benzénoïdes: Elles correspondent à des noyaux aromatiques. Apparaissent vers 250 nm, d’intensité beaucoup plus faible: 1000 <
 < 2000 Il s’agit toujours de transitions
< 2000 Il s’agit toujours de transitions  *
* - Bandes R comme radicalaires: On les retrouve quand on a dans la molécule des hétéro-atomes (S, P, O,…)
Elles correspondent à des transitions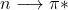
Les maxima d’absorption se situent à des longueurs d’onde supérieures à 250 nm
Elles sont d’intensités faibles < 100.
< 100.
A retenir:
| Bande | E, K | B | R |
| 10 000 | 1000 | 100 |
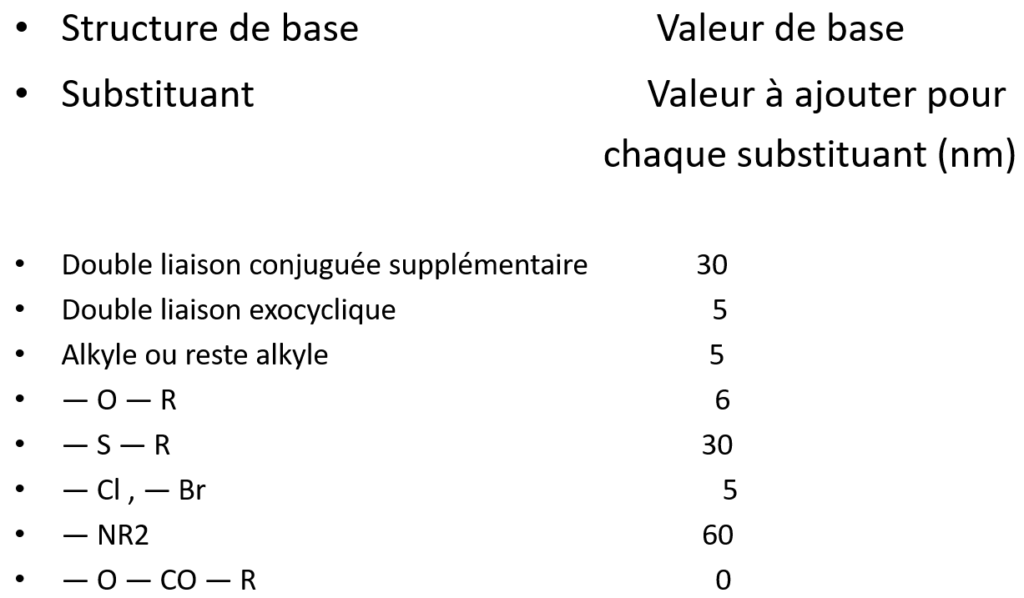
Règles de Woodward – Fieser
Ce sont des règles de calcul empiriques qui permettent de déterminer de façon approximative le maximum d’absorption d’une bande lorsque l’on connaît la structure d’une molécule.
L’inverse n’est pas vrai : avec les maxima, on ne peut pas déterminer la structure.
Quelques exemples :
| Composés éthyléniques: | \lambda max |
| Diène linéaire | 217 nm |
| Diène hétéroannulaire | 214 nm |
| Diène homoannulaire | 253 nm |
Facteurs modifiant les bandes
Les 2 principaux facteurs sont le pH et le solvant.
pH
Selon le pH, on peut assister à une modification de la structure de la molécule si elle possède des propriétés acido-basiques.
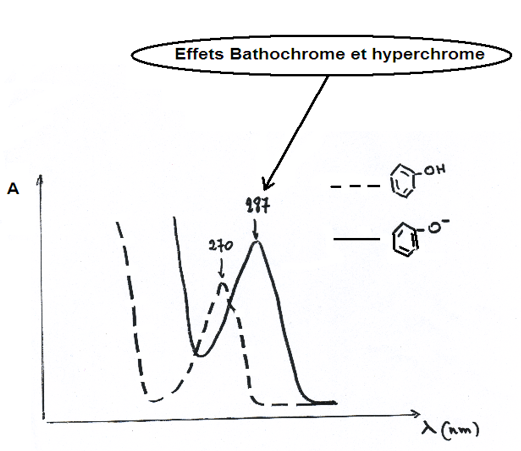
Exemple le plus classique: le phénol
Passage en milieu basique: effet bathochrome et hyperchrome.
On a affaire à une bande B.
Solvant
Lorsque la polarité du solvant change; l’espacement des niveaux d’énergie ![]() et
et ![]() change :
change :
- Transition
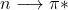
Stabilisation des électrons n en solvant polaire par création de liaison hydrogène .
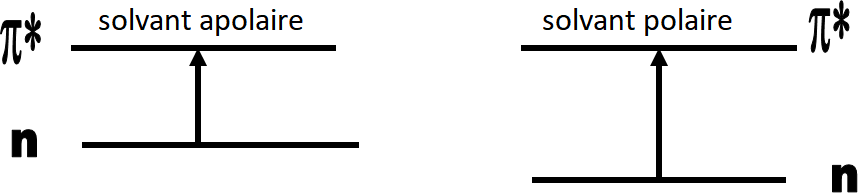
Exemple acétone dans : Eau (265 nm), Méthanol (270 nm), Chloroforme (276 nm).
- Transition
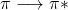 Stabilisation de l’orbitale
Stabilisation de l’orbitale 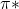 en solvant polaire car
en solvant polaire car 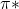 est plus polaire que
est plus polaire que 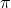
Share this content:
Table des matières