Bromométrie
Aspects généraux
La bromométrie est la méthode qui utilise le pouvoir oxydant du brome ou sa propriété de se fixer sur les doubles liaisons des composés organiques en milieu acide.
Les propriétés oxydantes de Br2 sont issues du KBrO3
(1) ![]()
Préparation des solutions titrées
BrO3–est pesée avec précision ![]()
- Le bromate de potassium KBrO3 est un étalon primaire (PM = 167,0)
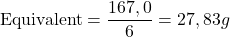
- On prépare en générale des solutions de 0,1 N de KBrO3
- On dissout 2,783 g de KBrO3 et 12 g KBr dans 1000 ml au moment de l’emploi,
- On acidifie le milieu par un acide fort
Applications
La bromométrie est très utile en analyse organique et moins importante en analyse minérale.
Phénols (thymol, résorcine…)
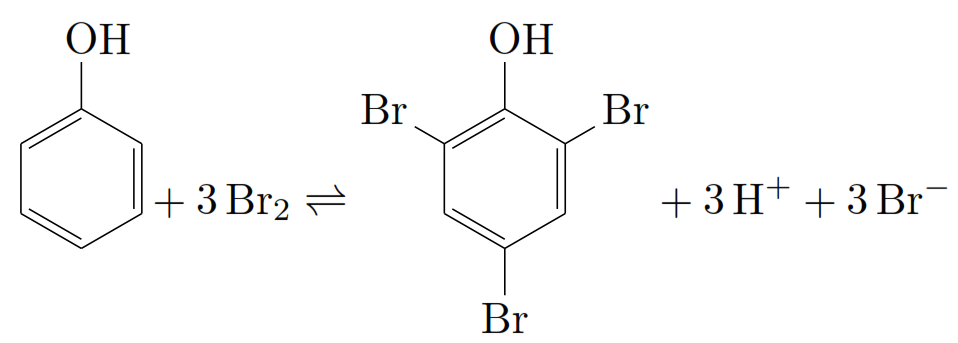
L’équivalent correspond au 1/6 de la molécule-gramme de phénol, les autres phénols réagissent de la même manière si les positions ortho et para sont libres.
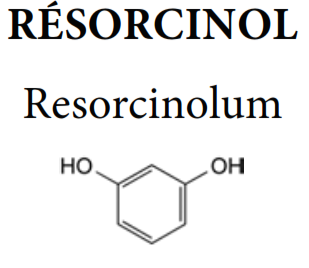
(Pharmacopée européenne 8.2)
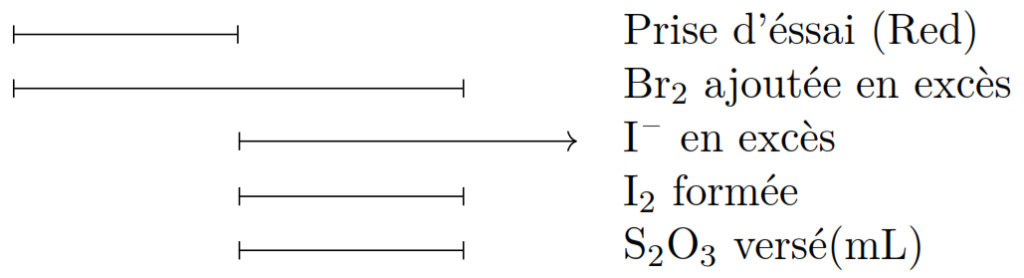
Dissolvez 0,500 g de résorcinol dans de l’eau et complétez à 250,0 mL avec le même solvant. Dans un ballon à bouchon rodé, introduisez 25,0 mL de cette solution, 1,0 g de KBr ,50,0 mL de KBrO3 0,0167 M , 15 mL de chloroforme et 15,0 mL d’acide chlorhydrique.
Bouchez le ballon, agitez et laissez reposer à l’obscurité pendant 15 min,en agitant de temps en temps. Ajoutez 10 mL d’une solution d’iodure de potassium à 100 g/L. Agitez énergiquement, puis laissez reposer pendant 5 min. Titrez par le Na2S2O3 0,1 M en présence de 1 mL de solution d’amidon.
1 mL de KBrO3 0,0167 M correspond à 1,835 mg de C6H6O2
Cations
Avec le Hydroxy-8-quinoléine:
L’hydroxy-8-quinoléine (voir figure ) ci-dessous donne un dérivé dibromé dans les mêmes conditions (position ortho bloquée).
(2) ![]()
Comme l’hydroxy-8-quinoléine précipite quantitativement avec divers métaux en donnant des chélates non chargés, il est possible de doser indirectement ces métaux, en ajoutant un excès connu de l’hydroxy-8-quinoléine.
Une partie précipite sous forme de complexe avec le métal, et l’excès du réactif complexant est doser par Br2.
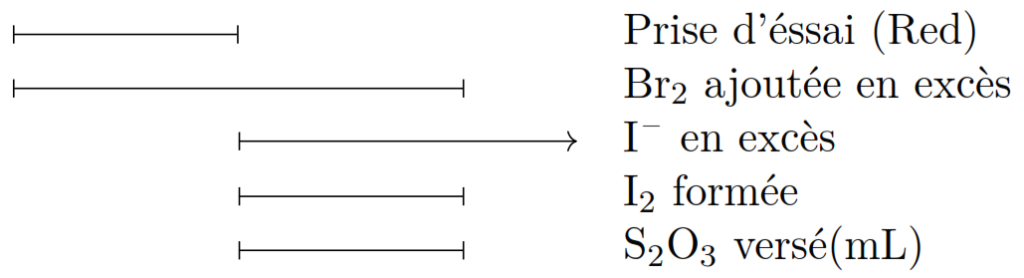
Voir schéma de dosage suivant:
Share this content:
Table des matières

