Émission atomique de flamme
Principe
La spectrophotométrie d’émission atomique est une méthode spectroscopique dédiée au dosage des métaux après excitation de ces derniers. En spectrophotométrie d’émission atomique on fournit de l’énergie sous forme thermique (flamme, plasma). On obtient d’abord des atomes à l’état de vapeur qui vont être ensuite excités. On mesure ensuite l’intensité du rayonnement émis lorsque ces atomes repassent à l’état fondamental.
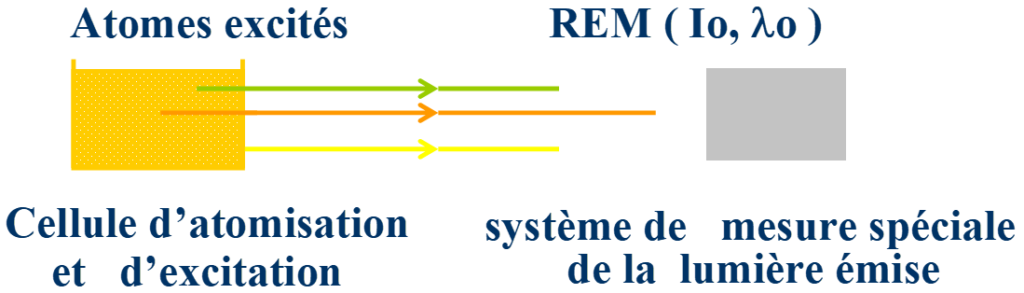
Il existe différents moyens pour apporter de la chaleur aux atomes :
- en utilisant une flamme: photométrie d’émission en flamme. (Méthode quantitative seulement)
- en utilisant un plasma : spectrophotométrie d’émission à couplage induit: ICP (inductively Coupled Plasma). (Méthode qualitative et quantitative).
- en utilisant un arc ou une étincelle électrique : spectrométrie d’émission d’arc ou d’étincelle électrique. (Méthode quantitative seulement).
Les phénomènes physico-chimiques
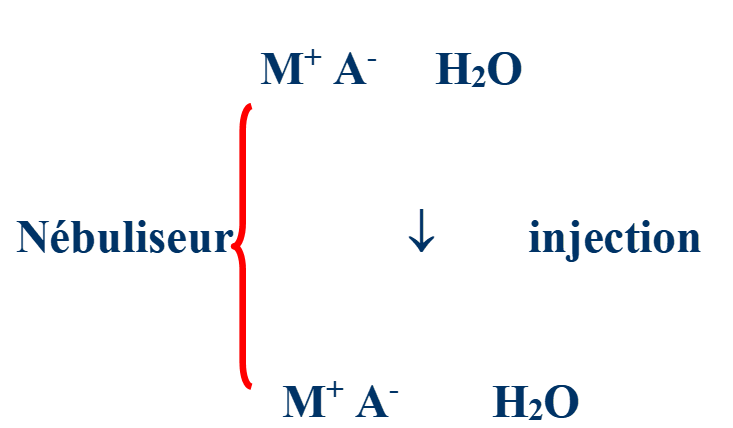

Appareillage
- Cas particulier: photomètre de flamme
- Cas général:
- Système d’atomisation: flamme
- Nébuliseur: même chose qu’en absorption atomique
- Brûleur de pré-mélange : flamme stable
- Gaz : mélange propane-air ou butane air
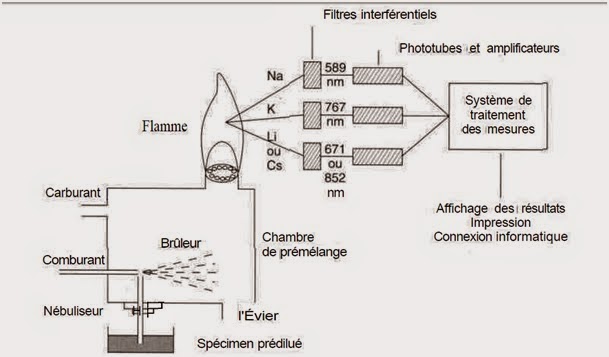
Système de mesure:
- Sélection du rayonnement: monochromateur ou filtres interférentiels
- Détection du signal : photodiodes pour mesurer le rayonnement ou photomultiplicateur
Mesure
Préparation de l’échantillon
On travaille sur des solutions diluées.
Dosage
Étalonnage externe
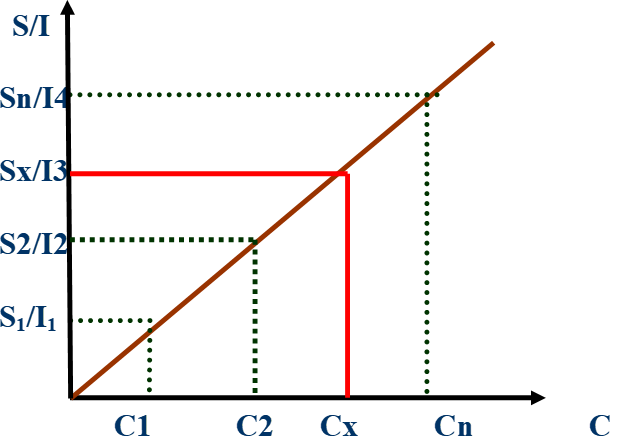
On réalise une série d’étalons de concentration Cl, C2, … Cn.
On mesure les signaux S1, S2, … Sn émis par ces étalons et le signal Sx émis par l’échantillon de concentration inconnue Cx .
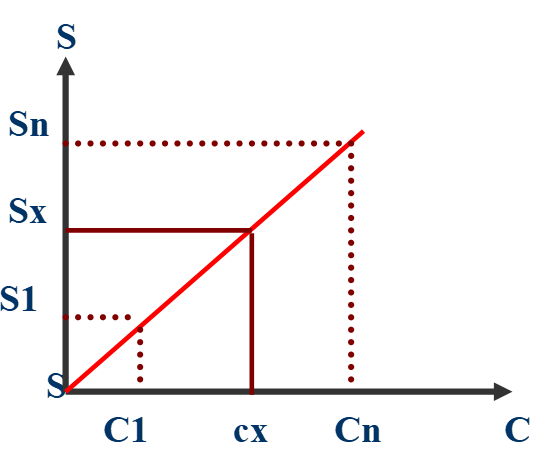
Par la méthode des moindres carrés on calcule la droite de régression (Figure ).
Étalonnage interne
on ajoute aux solutions étalons
Cl, C2, … Cn et à l’échantillon Cx , une quantité constante d’un autre élément que celui à doser (étalon interne).
Donc on fait des mesures à deux longueurs d’ondes différentes.
On mesure simultanément le signal à la longueur d’onde de l’élément. On obtient S1, S2, … Sn, Sx.
et à la longueur d’onde de la lumière émise par l’étalon interne.
on obtient: I1, I2, … In, Ix.
Il faut donc deux détecteurs (Figure).
On fait le rapport:
![]()
S’il y a une variation de la température de la flamme. ![]() varie, mais
varie, mais ![]() varie aussi, on est donc à l’abri:
varie aussi, on est donc à l’abri:
- de l’instabilité de la flamme
- de la variation du rendement de nébulisation.
L’étalon interne doit avoir les caractéristiques suivantes:
- potentiel d’excitation voisin de celui de l’élément à doser
- une longueur d’onde d’émission voisine de celle de l’élément à doser
Par exemple : pour doser Na et K l’étalon interne sera Li.
![]()
Interférences spectrales
Self absorption: des atomes à l’état fondamental sont susceptibles d’absorber le rayonnement émis par les atomes excités: on a une erreur par défaut. Cette absorption est d’autant plus intense que la longueur d’onde émise est plus proche de la valeur théorique.
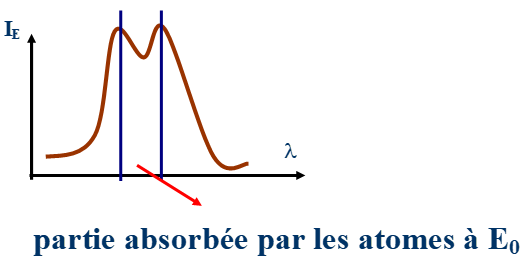
C’est le phénomène de renversement des raies. Il est d’autant plus important que la concentration est grande, d’ou l’intérêt de travailler sur des solutions diluées.
Applications
Aux alcalins et aux alcalino-terreux.
Biologie
Dosage du Na et K. Aujourd’hui, ces méthodes commencent à être remplacées par potentiométrie directe à électrodes sélectives.
Pharmacie
Dosage du litium (Li) sérique ou globulaire par photométrie de flamme. Cette méthode permet de surveiller les patients en cours de traitement par les sels de lithium.
Share this content:
Table des matières